Новости дерматологии
Исследование потенциальных низкомолекулярных биомаркеров рака кожи: исследование на здоровых добровольцах
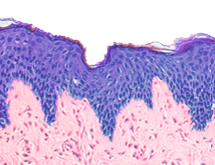
Злокачественные опухоли кожи излечимы у большинства пациентов, если диагностика и удаление происходит до установления метастатического фенотипа опухоли. На сегодняшний день визуальный осмотр с последующей биопсией является золотым стандартом диагностики. Но по ряду некоторых исследований на ранней стадии визуальный диагностический подход имеет ограниченную специфичность (<30%) и чувствительность (около 84%). Это означает, что из 100 случаев меланомы, в отношении которых было принято решение об удалении, только 30 являются меланомами. Чувствительность 84% означает, что 16% случаев истинной меланомы будут диагностированы неправильно. Недовольство таким положением вещей приводит к внедрению диагностических методик (дерматоскопия, конфокальная микроскопия и др.), специфичность и чувствительность которых зависит от навыков врача. Шведские ученые разрабатывают новую методику, основанную на определении молекул, количество которых были бы присущи меланоме и не встречались у здоровых лиц. Дело в том, что растущие к поверхности кожи клетки меланомы в 2-4-недельный период могут выделять опухолевые биомаркеры с высокой молекулярной массой. Данный срок связан с длительностью продвижения кератиноцитов на поверхность кожи. В свою очередь микроокружение опухоли может гораздо быстрее экспонировать на поверхности кожи с низкомолекулярные биомаркеры. Низкомолекулярные соединения <500 Да могут проникать через роговой слой и достигать поверхности кожи в течение нескольких часов. В ходе химических реакций в киноурениновом метаболическом пути триптофан превращается в биологически активные метаболиты, включая кинуренин, тремя ферментами - индоламин-2,3-диоксигеназами-1 и 2 и триптофан-2,3-диоксигеназой. Сообщается, что экспрессия первого фермента повышается при многих злокачественных новообразованиях, таких как рак легкого, почечно-клеточный рак, меланома. Повышенная экспрессия фермента приводит к истощению триптофана и накоплению кинуренина, что приводит к изменению соотношения триптофан/кинуренин в микроокружении и в плазме пациента с меланомой, что коррелирует с ожидаемой выживаемостью пациента. Поскольку эти вещества являются низкомолекулярными соединениями и способны диффундировать через кожный барьер, то шведские ученые видят большие перспективы в их определении на поверхности кожи. Они показали, что при сравнении кожи здоровых добровольцев до и после изменения активности фермента наблюдается уменьшение отношения триптофан/кинуренин в 80–100 раз. Кроме того, исследование показало, что используемое для контроля отношение фенилаланин/триптофан также менялось в 20-30 раз. Авторы полагают, что эти результаты, наряду с высокой воспроизводимостью, могут применяться не только для диагностики, но и для неинвазивной оценки терапии меланомы.
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
Эффективность и безопасность геля бердазимера против контагиозного моллюска: рандомизированное клиническое исследование
Контагиозный моллюск (КМ) — распространенная, стойкая и высококонтагиозная кожная инфекция, вызываемая поксвирусом. Ежегодно только в США им болеют около 6 миллионов человек с наибольшей заболеваемостью среди детей в возрасте от 1 до 14 лет. Инфекция контагиозного моллюска, как правило, проходит сама по себе, но может сохраняться от месяцев до лет, создавая нагрузку на здравоохранение и вызывая проблемы с качеством жизни, требующие лечения. Лечение также может быть оправдано из-за высокой контагиозности высыпаний и опасения заразить сверстников или членов семьи. Кроме того, внешне видимые поражения могут быть связаны с дискомфортом и психосоциальной стигматизацией, а после разрешения могут остаться шрамы. Оксид азота действует как кратковременный иммуномодулятор и как прямой антимикробный агент широкого спектра действия, обеспечивающий локальный иммунитет против чужеродных организмов. Оксид азота выполняет регуляторные функции, которые влияют на NF-?B, продукцию цитокинов и апоптоз, вероятно, посредством нитрозилирования белков. Также он обладает цитотоксическими функциями, которые влияют на репликацию вируса посредством реактивных молекул кислорода и/или азота. Но сложности с хранением и доставкой оксида азота к очагу инфекции или воспаления ограничивают его местное применение. 10,3% гель бердазимера - это новый препарат для местного применения, высвобождающий оксид азота. Совместное введение двух компонентов, нового химического соединения бердазимера натрия (гель) и гидрогеля, функционирующего в качестве донора протонов, способствует высвобождению оксида азота из макромолекулы бердазимера натрия. Американские исследователи сообщают об эффективности и безопасности данного геля против КМ. В своё исследование они отобрали 891 пациента в возрасте 6 месяцев и старше, с нормальным иммунитетом и имевших от 3 до 70 возвышающихся очагов КМ. Пациенты не получали какое-либо лечения в течение 14 дней до начала нанесения геля. Пациенты или лица, осуществляющие уход, наносили гель 1 раз в день тонким слоем. Если на контрольных визитах подтверждалось, что очаги разрешились, то лечение прекращалось, а пациенты наблюдались на предмет рецидива или появления новых очагов до 24-й недели. Контрольной точкой была выбрана 12 неделя. В группу бердазимера было отобрано 444 пациента со средним возрастом 6,6 лет, среди которых 228 (51,4%) мужчин; в группу плацебо - 447 пациентов со средним возрастом 6,5 лет; 234 (52,3%) женщины. В группе пациентов, получавших лечение, у 88,5% (393 пациента) в группе бердазимера и у 88,8% (397 пациентов) в группе геля-носителя на 12-й неделе был проведен подсчет поражений. В группе лечения было достигнуто полное исчезновение очагов у 32,4% (144 пациента) и у 19,7% (88 пациентов) в группе контроля. Нежелательные явления, приведшие к прекращению лечения, наблюдались у 4,1% (18 пациентов) в группе бердазимера и у 0,7% (3 пациента) в группе плацебо. Наиболее распространенной местной кожной реакцией была эритема легкой или средней степени тяжести.
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
3 фаза долгосрочного открытого периода наблюдения за безопасностью и эффективностью белимумаба у пациентов с СКВ в ??Китае
Системная красная волчанка (СКВ) представляет собой хроническое воспалительное аутоиммунное заболевание, которое обычно проявляется рядом специфических проявлений, в том числе мультисистемным микрососудистым воспалением с образованием аутоантител. Кроме того, что болезнь клинически гетерогенна, она имеет и расовые различия, влияющие на прогрессирование и распространенность. Так СКВ более распространена и тяжелее протекает в неевропеоидной популяции, чем в европеоидной популяции. В Китае СКВ поражает 97,5–100 человек на 100 000 населения. Несмотря на достижения в диагностике и лечении СКВ, у многих пациентов наблюдается прогрессирование заболевания, а длительное использование стандартной терапии часто связано с токсичностью и значимыми побочными эффектами. В терапии СКВ, как и в терапии многих аутоиммунных болезней, применяют моноклональные антитела. Белимумаб представляет собой моноклональное лямбда-антитело иммуноглобулина G1 человека, которое связывается со стимулятором В-лимфоцитов (BLyS) и ингибирует его биологическую активность. Предыдущие исследования белимумаба для внутривенного применения показали эффективность при СКВ в сочетании со стандартной терапией. В Китае было проведено исследование препарата выходящее за привычные пределы в 52 недели. Сначала пациенты проходили тот самый 52-недельный двойной слепой плацебо-контролируемый период исследования, затем все желающие могли продолжить лечение белимумабом в дозе 10 мг/кг в/в каждые 28 дней в сочетании со стандартной терапией в течение 6 лет. 84,7% (359 из 424) пациентов сообщили о нежелательных явлениях на фоне лечения. Наиболее частыми из них были инфекции верхних дыхательных путей (35,4%). В целом частота всех нежелательных явлений была стабильной или снижалась с течением времени. Во время лечения белимумабом доля респондеров c индексом ответа SRI-4 увеличилась с 54,9% на 1-ом году до 80,5% на 5-ый год. Точно так же доля пациентов со снижением шкалы активности волчанки SELENA-SLEDAI увеличилась с 55,9% до 81,9% на 5-ый год. Ряду пациентов на фоне лечения стало возможно снизить ежедневную дозу преднизолона. Эти результаты, как согласуются с предыдущими исследованиями, так и подтверждают положительное соотношение пользы и риска лечения белимумабом в качестве дополнения к стандартной терапии.