Новости дерматологии
Кривые частоты солнечных ожогов в течение жизни и связанные с ними риски меланомы кожи и плоскоклеточного рака
В Норвегии увидело свет исследование, в котором изучались закономерности солнечных ожогов в разные возрастные периоды и их связь с меланомой и плоскоклеточным раком кожи (ПКР). Преимуществом данного исследования перед другими является долгосрочный период наблюдения, а не просто сравнение пациентов, получивших солнечный ожог в одном возрастном периоде с контрольной группой. Исследование оценивало данные опросников за период 1991-2018. В исследование после исключения женщин с темной кожей, распространенной меланомой или ПКР, эмигрировавших или умерших до даты возврата анкеты были отобраны 168 553 женщины, родившиеся с 1927 по 1965. Было подсчитано среднее количество годовых солнечных ожогов в каждом десятилетии и составлены кривые (траектории) этих ожогов: стабильно низкая (мало ожогов), низкая-умеренная-низкая (мало ожогов в детстве и старшем возрасте), низкая-высокая (мало ожогов в детстве, много в зрелом возрасте), высокая-низкая (много в детстве и мало в зрелом возрасте) и стабильно высокая (много ожогов в течение жизни). В дальнейшем было проведено сравнение разных кривых со стабильно низкой траекторией: 1,5-кратное отношение рисков для развития меланомы и ПКР отчетливо наблюдалось среди женщин младше 40 лет со стабильно высокой траекторией и траекторией от высокой к низкой. Другие траектории показали повышенный риск, хотя в целом более слабый и в основном полученные оценки не были статистически значимыми. Это когортное исследование показало, что высокая частота солнечных ожогов в течение жизни была связана с повышенным риском развития меланомы и плоскоклеточного рака. Кроме того, солнечные ожоги в детстве особенно важны для последующего риска развития этих видов рака кожи.
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
Влияние биотина может приводить к ложноотрицательным результатам специфических IgE у пациентов с анафилаксией
Нормальные концентрации биотина в плазме колеблются от 0,1 до 0,8нг/мл у взрослых, принимающих рекомендуемую суточную дозу 30 мкг с пищей. Как безрецептурный, так и оправданный с медицинской точки зрения прием биотина сопряжен со значительным риском изменений в рутинных медицинских лабораторных тестах с использованием биотин-стрептавидиновой реакции. Пероральные дозы 20 мг биотина в день приводят к максимальной концентрации в плазме 184 нг/мл у здоровых взрослых. При дозе 300 мг/сут, которая используется врачами при рассеянном склерозе, были пиковые концентрации в плазме достигали 824 ± 303 нг/мл. Анализы на основе биотина используются для выявления аллерген-специфических IgE (cIgE) при диагностике аллергии, следовательно прием биотина может менять эти показатели. Международная группа врачей провела исследование того, как менялись значения cIgE у пациентов с анафилактической реакцией на пищевые и вдыхаемые аллергены. При комплексном анализе всех 18 образцов пациентов с анафилактическими заболеваниями наблюдалось значительное влияние концентраций биотина (оценивались 184 и 300 нг/мл) на значения IgE. Например, биотина в концентрации 300 нг/мл было достаточно, чтобы вызвать значительное снижение сIgE, что сделало все результаты образцов ложноотрицательными. Концентрация 184мг/нл делала ложноотрицательными до половины результатов. Чтобы избежать потенциального негативного воздействия результатов анализов, лаборатории и врачи должны быть осведомлены о деталях приема лекарств пациентами.
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
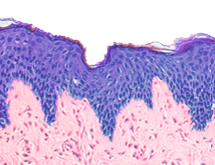
Лечение пемфигоидного красного плоского лишая с помощью месалазина: новое применение этого препарата
Пемфигоидный красный плоский лишай (ПКПЛ) был впервые описан Капоши в 1892. Он характеризуется обширным образованием пузырей на нормальной коже наряду с ранее существовавшими типичными высыпаниями КПЛ. ПКПЛ отличается от буллезной формы КПЛ, тем что пузыри образуются на видимо здоровой коже, а не поверх типичных высыпаний КПЛ. Патогенез образования пузырей обусловлен образованием аутоантител IgG против антигенов буллезного пемфигоида BP180 и 230 и антигена 200 кДа. Лечение включает дапсон, системные стероиды, циклоспорин, азатиоприн и, в последнее время, биологические препараты, включая устекинумаб, с различной степенью успеха. Из Индии пришло сообщение об успешном лечении ПКПЛ с помощью месалазина. У 58-летнего мужчины в течение последних 5 лет наблюдались множественные фиолетовые, зудящие папулы и бляшки на тыльной поверхности кистей и стоп, а также поражения полости рта и половых органов. Рецидивирующие пузырные поражения отмечались на здоровой коже, преимущественно на конечностях и в небольшом количестве на туловище. Диагноз был подтвержден гистологически. Пациенту был назначен месалазин по 800 мг 3 раза в день. Буллезные поражения разрешились в течение 2 недель, рецидива не наблюдалось в течение 6 месяцев. В качестве адъювантной терапии гипертрофических бляшек применяли 0,05% бетаметазона дипропионат. У пациента не наблюдалось серьезных побочных реакций.