Новости дерматологии
Упадацитиниб в сочетании с топическими кортикостероидами при атопическом дерматите
Упадацитиниб - селективный обратимый ингибитор янус-киназы (JAK)-1. Является более мощным ингибитором JAK1 по сравнению с JAK2 и JAK3. При исследовании активности на культурах клеток с целью прогнозирования фармакодинамического ответа in vivo упадацитиниб демонстрировал селективность в отношении JAK1 в 50-70 раз выше, чем в отношении JAK2, и более чем в 100 раз выше, чем в отношении JAK3. Ранее из Японии приходили данные об его эффективности в сочетании с топическими кортикостероидами (ТКС) при лечении атопического дерматита (АтД) в ходе 16-недельного наблюдения. Теперь поступили данные о 52-недельном наблюдении от группы международных исследователей из 171 клинического центра. Исследование имело 35-дневный период скрининга, 16-недельный двойной слепой период, повторную рандомизацию и наблюдение до 52-ой недели. В исследовании приняли участие пациенты в возрасте от 12 до 75 лет с АтД средней и тяжелой степени (?10% пораженной площади поверхности тела, индекс площади и тяжести экземы (EASI) ?16, глобальная оценка исследователя для АтД (vIGA-AD) ?3 и числовая шкала оценки зуда (WP-NRS) ?4). Они были рандомизированы в соотношении 1:1:1 для приема упадацитиниба 15 мг 1 раз в сутки + ТКС, упадацитиниба 30 мг + ТКС или плацебо + ТКС. На 16-й неделе в общей сложности 283 пациента из последней группы были повторно рандомизированы — 144 в группу упадацитиниба 15 мг + ТКС и 139 — в группу упадацитиниба 30 мг + ТКС. Остальные пациенты оставались в своих прежних группах. Эффективность упадацитиниба 15 мг + ТКС и упадацитиниба 30 мг + ТКС на 16-й неделе сохранялась и до 52-й недели. На 52-й неделе доля пациентов, получавших упадацитиниб 15 мг + ТКС и упадацитиниб 30 мг + ТКС, EASI75 (снижение EASI на 75%) составили 50,8% и 69,0% соответственно; 33,5% и 45,2%, соответственно, имели vIGA-AD 0/1; и 45,3% и 57,5%, соответственно, испытали улучшение по шкале WP-NRS. Упадацитиниб + ТКС хорошо переносился в течение 52 недель. Никаких новых побочных эффектов не наблюдалось, о смертельных случаях не сообщалось; серьезные неблагоприятные сердечно-сосудистые события и венозные тромбоэмболические события были не частыми (?0,2/100 пациенто-лет). Подводя итог, авторы считают, что результаты 52 недель наблюдения еще раз подтверждают потенциал упадацитиниба + ТКС как хорошо переносимого и эффективного варианта долгосрочного лечения умеренного или тяжелого АтД у взрослых и подростков.
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
Риск инвазивной плоскоклеточной карциномы кожи после различных видов лечения актинического кератоза
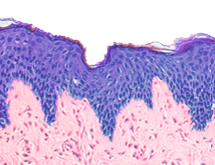
Распространенность актинического кератоза (АК) во всем мире колеблется от 11% до 60%, и является заболеванием, которое часто диагностируется и лечится дерматологами и врачами общей практики. Наиболее важной причиной для лечения является предполагаемое снижение риска развития инвазивной плоскоклеточной карциномы кожи (ПКК). В Нидерландах провели исследование, в котором сравнивались 4 метода лечения АК. В это многоцентровое рандомизированное исследование были включены 624 пациента (89,4% мужчин; средний возраст 73 года) с минимум 5 АК на площади от 25 до 100 см2 на голове. Пациентам случайным образом назначали 1 из 4 различных видов лечения в соотношении 1:1:1:1: 5% крем фторурацила, 5% крем имиквимода, ФДТ с метиламинолевулинатом и 0,015% гель мебутата ингенола. Пациенты проходили лечение с 2014 по 2017, отдаленное наблюдение проводилось с 2019 по 2020. Первичным результатом была доля пациентов с ПКК в целевой области во время последующего наблюдения. Вторичными результатами были связи между риском инвазивного ПКК и определенными потенциальными прогностическими факторами (тип лечения, тяжесть АК, наличие в анамнезе немеланомного рака кожи и дополнительное лечение). Гистологически подтвержденный ПКК в целевой области был диагностирован у 26 пациентов. Из этих 26 пациентов 4 находились в группе фторурацила, 10 — в группе имиквимода, 6 — в группе ФДТ и 6 — в группе ингенола мебутата. Все ПКК наблюдались у пациентов с АК II и III степени. 4 были локализованы в ранее существовавшем поражении АК III степени, 14 — в ранее существовавшем поражении АК II степени и 3 — вне поражения АК, в 5 случаях не было неясно, были ли они расположены в ранее существовавшем АК. У 7 пациентов ПКК развилась в течение 12 месяцев после окончания лечения. В общей популяции исследования 4-летний риск ПКК после лечения составил 3,7%
- Чтобы увидеть комментарии, войдите или зарегистрируйтесь
Прогностическое и прогностическое значение ?-блокаторов в исследовании III фазы EORTC 1325/KEYNOTE-054
Исследования in vitro показали, что экспрессия ?-адренорецепторов повышается при различных видах рака. Активация ?-адренорецепторов вносит вклад в проонкогенную микросреду благодаря своей роли в апоптозе, воспалении, ангиогенезе, репарации ДНК и клеточном иммунитете. Среди 29 наиболее распространенных видов рака человека меланома сильнее всего экспрессирует ?-адренорецепторы, включая отдельные подтипы рецепторов ?1, ?2 и ?3. Считается, что все 3 подтипа играют роль в развитии и прогрессировании меланомы, способствуя высвобождению проонкогенных цитокинов и металлопротеаз и уменьшая размножение Т-клеток и цитотоксичность. ?-адреноблокаторы представляют собой хорошо переносимый и часто назначаемый класс препаратов с целым рядом показаний. Большой интерес представляет прогностический эффект использования ?-блокаторов на эффективность иммунотерапии. Иммунотерапия изменила лечение меланомы и в настоящее время является стандартом лечения как при наличии метастазов, так и в качестве адъювантной терапии при удалении опухоли III стадии. Доклинические исследования показали, что ингибиторы PD-1 более эффективны у мышей в сочетании с фармакологическими ?-блокаторами. Ретроспективное клиническое исследование в Соединенных Штатах с участием 195 пациентов с метастатической меланомой, получавших один или комбинацию иммунотерапевтических агентов анти-PD-1, анти-CTLA-4 и IL-2, а также неселективные ?-адреноблокаторы продемонстрировало улучшение общей выживаемости. Настоящее международное исследование III фазы EORTC-1325/KEYNOTE-054 было направлено на дальнейшее изучение прогностической и прогностической ценности ?-блокаторов и пембролизумаба при резецированной меланоме III стадии высокого риска. Пациенты с резецированной меланомой стадии IIIA, IIIB или IIIC и регионарной лимфаденэктомией получали 200 мг пембролизумаба в качестве адъювантной терапии (n = 514) или плацебо (n = 505) каждые 3 недели в течение одного года или до появления рецидива или неприемлемой токсичности. При среднем периоде наблюдения в 3 года пембролизумаб увеличивал безрецидивную выживаемость по сравнению с плацебо. Использование ?-блокаторов определялось как пероральное введение любого ?-блокатора в течение 30 дней после рандомизации. ?-адреноблокаторы не оказали независимого прогностического влияния на безрецидивную выживаемость. Отношение рисков безрецидивной выживаемости связанный с пембролизумабом по сравнению с плацебо, составило 0,34 среди принимавших ?-блокаторы и 0,59 среди тех, кто не принимал ?-блокаторы. Авторы полагают, что их результаты не ставят крест на использовании ?-блокаторов. Возможным направлением работы может быть изучение тех или иных селективных препаратов в сочетании с другими иммунотерапевтическими агентами.